Bài 1. (Trang 25 SGK Hóa 9)
a) Có phải tất cả các chất kiềm đều là bazơ không? Dẫn ra công thức hóa học của ba chất để kiềm để minh họa.
b) Có phải tất cả các bazơ đều là chất kiềm không? Dẫn ra công thức hóa học của ba chất để kiềm để minh họa.
Hướng dẫn giải bài 1:
a) Vì kiềm là một loại bazơ tan được trong nước nên tất cả các chất kiềm đều là bazơ.
Thí dụ: NaOH, KOH, Ba(OH)2.
b) Vì không phải mọi bazơ đều tan trong nước nên không phải tất cả các bazơ đều là chất kiềm.
Thí dụ: Các bazơ Cu(OH)2, Mg(OH)2, Fe(OH)3... không phải là chất kiềm.
Bài 2. (Trang 25 SGK Hóa 9)
Có những bazơ sau: Cu(OH)2, NaOH, Ba(OH)2. Hãy cho biết những bazơ nào
a) Tác dụng được với với dung dịch HCl. b) Bị nhiệt phân hủy.
c) Tác dụng được CO2. d) Đổi màu quỳ tím thành xanh.
Hướng dẫn giải bài 2:
a) Tất cả các bazơ đều tác dụng với axit HCl:
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
NaOH + HCl → NaCl + H2O
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
b) Chỉ có Cu(OH)2 là bazơ không tan nên bị nhiệt phân hủy:
Cu(OH)2 → CuO + H2O
c) Những bazơ tác dụng với CO2 là NaOH và Ba(OH)2.
NaOH + CO2 → Na2CO3 + H2O
Ba(OH)2 + CO2 → BaCO3 + H2O
d) Những bazơ đổi màu quỳ tím thành màu xanh là NaOH và Ba(OH)2.
Bài 3. (Trang 25 SGK Hóa 9)
Từ những chất có sẵn là Na2O, CaO, H2O. Hãy viết các phương trình hóa học điều chế các dung dịch bazơ.
Hướng dẫn giải bài 3:
Phương trình hóa học điều chế các dung dịch bazơ:
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2
Bài 4. (Trang 25 SGK Hóa 9)
Có 4 lọ không nhãn, mỗi lọ đựng một dung dịch không màu sau: NaCl, Ba(OH)2, NaOH, Na2SO4. Chỉ được dùng quỳ tím, làm thế nào nhận biết dung dịch đựng trong mỗi lọ bằng phương pháp hóa học? Viết các phương trình hóa học.
Hướng dẫn giải bài 4:
Lấy từ mỗi lọ một mẫu hóa chất (gọi là mẫu thử) để làm thí nghiệm nhận biết.
Cho quỳ tím vào mẫu thử từng chất và quan sát, thấy:
Những dung dịch làm quỳ tím đổi màu là: NaOH và Ba(OH)2, (nhóm 1).
Những dung dịch không làm quỳ tím đổi màu là: NaCl, Na2SO4 (nhóm 2).
Để nhận ra từng chất trong mỗi nhóm, ta lấy một chất ở nhóm (1), lần lượt cho vào mỗi chất ở nhóm (2), nếu có kết tủa xuất hiện thì chất lấy ở nhóm (1) là Ba(OH)2 và chất ở nhóm (2) là Na2SO4. Từ đó nhận ra chất còn lại ở mỗi nhóm.
Phương trình phản ứng: Ba(OH)2 + Na2SO4 → BaSO4 + NaOH
Hoặc các em xem theo sơ đồ hướng dẫn sau
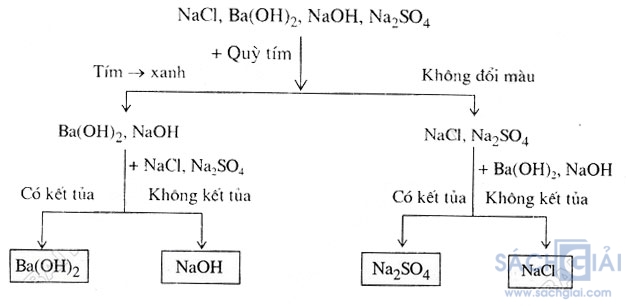
Bài 5. (Trang 25 SGK Hóa 9)
Cho 15,5 gam natri oxit Na2O tác dụng với nước, thu được 0,5 lít dung dịch bazơ.
a) Viết phương trình hóa học và tính nồng độ mol của dung dịch bazơ thu được.
b) Tính thể tích dung dịch H2SO4 20% có khối lượng riêng 1,14 g/ml cần dùng để trung hòa dung dịch bazơ nói trên.
Hướng dẫn giải bài 5:
Số mol Na2O = 15,5:62 = 0,25 mol
a) Khi cho Na2O xảy ra phản ứng, tạo thành phản ứng dung dịch có chất tan là NaOH.
Na2O + H2O → 2NaOH
0,25 → 0,5 (mol)
500 ml = 500/1000= 0,5 lít; CM, NaOH = 0,5/0,5 = 1M.
b) Phương trình phản ứng trung hòa dung dịch:
2NaOH + H2SO4 → Na2SO4 + 2H2O
Pứ 0,5 → 0,25 0,25 (mol)
mH2SO4 = 0,25×98 = 24,5 g
mdd H2SO4 = 24,5.100/20= 122,5 g
mdd, ml = mdd,g = Dg/ml = 122,5/1,14 ≈ 107,5 ml